Analyser som påvirkes mest av hemolyse er:
Prosedyre for venøs blodprøvetaking
v. 4.11
1. Hensikt
Hensikten med prosedyren er å etablere standardiserte retningslinjer for å:
-
redusere antall preanalytiske feil
-
ivareta pasientens og prøvetakers sikkerhet
-
sikre god kvalitet på prøvematerialet
Blodprøver brukes til diagnostikk og behandling av pasienter. Dermed er det viktig at prøven gir et korrekt bilde av pasientens helsetilstand. Det er viktig å ha tilstrekkelig kunnskap om forholdene rundt prøvetakingen, samt å innarbeide gode rutiner og praktiske ferdigheter. Prosedyren skal sikre at prøvetaker utfører blodprøvetaking på en etisk og faglig forsvarlig måte, og at prøvene leveres for analysering så raskt som mulig.
2. Omfang
Prosedyren omhandler venøs blodprøvetaking hos barn og voksne. Den gjelder for både primærhelsetjenesten og spesialisthelsetjenesten, og skal benyttes av helsepersonell med relevant opplæring i blodprøvetaking.
3. Definisjoner
Avdeling for medisinsk biokjemi = AMB
Total parenteral ernæring = TPN
4. Ansvar
Prøvetaker har ansvar for å ta rekvirerte blodprøver i henhold til gjeldende prosedyrer.
Prøver sendes via rørpost Rørpost, sending, mottak og pakking av patron (Ikke tilgjengelig). Ved problemer med rørpost, leveres prøvene til ekspedisjon AMB i 1. etasje, B-bygget.
5. Beskrivelse
Blodprøver benyttes blant annet til:
-
diagnostisering av sykdom
-
vurdering av sykdommens alvorlighetsgrad
-
oppfølging av behandling og behandlingsrespons
-
screening av tilsynelatende friske personer
Pasienten har krav på profesjonell behandling. Dette innebærer å bli møtt med respekt, høflighet og omsorg.
Helsehjelp er i utgangspunktet frivillig, og pasienten skal – så langt det er mulig – gi samtykke til blodprøvetaking.
Dersom pasienten nekter prøvetaking, skal prøvetaker kontakte pleiepersonell eller rekvirerende lege for vurdering av nødvendighet og eventuell tilrettelegging for å berolige pasienten.
Blodprøver skal ikke tas med tvang på myndige pasienter med mindre prøvesvaret er livsnødvendig. Prøvetaker, lege og pleiepersonell skal samarbeide for å gjennomføre prøvetaking uten bruk av tvang.
Prøvetaker skal ikke delta i prøvetaking dersom situasjonen oppleves som et overgrep mot pasienten.
6. Smitte- og personvern
6.1 Pasientens sikkerhet
Basale smittevernsrutiner skal alltid følges for å unngå overføring av smitte. Hånddesinfeksjon eller håndvask med såpe og vann er det viktigste enkelttiltaket for å forebygge smittespredning og skal utføres mellom hver pasient.
Desinfeksjon av stikksted
Ved blodkultur, på kreftavdelinger (D4/D5) og hos pasienter i beskyttende isolasjon skal klorhexidinsprit 5 mg/mL benyttes til huddesinfeksjon. Desinfeksjonsmiddelet påføres i tilstrekkelig mengde slik at hele stikkstedet er fullstendig dekket. Området skal lufttørke i 30 sekunder før venepunksjon utføres.
På sengepost skal pussbekken benyttes til oppbevaring av prøvetakingsutstyr. Dersom pussbekken plasseres i uren sone (for eksempel på pasientens seng eller nattbord), skal det legges rent tørkepapir under for å redusere risiko for kontaminasjon.
Helsepersonell har taushetsplikt. Pasientopplysninger skal håndteres konfidensielt og sikres mot uautorisert innsyn til enhver tid:
-
Prøvetakingslister skal snus slik at pasientopplysninger ikke er synlige for uvedkommende
-
Etiketter skal dekkes til når de ikke er i bruk
-
Dokumenter med pasientopplysninger skal oppbevares i hyllen under trallen når de ikke benyttes aktivt
-
Ubrukte etiketter med pasientopplysninger skal makuleres umiddelbart
6.2 Prøvetakers sikkerhet
Venepunksjon innebærer risiko for eksponering for smitte, enten ved stikkskade eller ved direkte kontakt med blod. Ved stikkskade skal gjeldende prosedyre Stikkskade - oppfølging.
Ved kjent blodsmitte skal informasjon om smittefare påføres prøvetakingslisten eller bestillingen av hensyn til prøvetaker og laboratoriepersonell. Prøverørene skal merkes med gul tusj.
Hansker skal benyttes ved forventet kontakt med blod, ikke-intakt hud eller annet potensielt infeksiøst materiale. Hansker skal også brukes ved kontakt med pasienter i isolat (kontakt-, dråpe- eller luftsmitte), Prøvetaking: Isolerte pasienter.
Ved prøvetaking på smitterom skal gjeldende prosedyre for prøvetaking av isolerte pasienter følges, Isolerte pasienter. Prøver tatt i urent miljø skal ikke sendes til laboratoriet uten at de er tilstrekkelig desinfisert.
Påkledningsinstruks som er angitt på døren til smitterommet skal følges. Ved avkledning skal prosedyre for Isolering - på og avkledning av personlig beskyttelsesutstyr følges. Avdelingen har ansvar for at smitterommet er utstyrt med staseslange, kanylebokser og nødvendig smittevernsutstyr.
Alle holdere er engangsutstyr og skal umiddelbart etter bruk kastes samlet i gul avfallsboks uten at nål og holder demonteres. Dette gjelder også holdere brukt til blodkultur.
7. Generelle forberedelser
Prøvetakingslistene skal kontrolleres for prøver som skal prioriteres (for eksempel medikamentspeil, morgenkortisol eller fastende prøver). Det skal også sjekkes om bestillingen krever spesialglass eller spesialutstyr. Eventuelle kommentarer fra rekvirent skal gjennomgås for relevant informasjon om prøvetakingen.
7.1 Pasientforberedelser
7.1.1 Faste
Noen analyser krever at prøven tas fastende, det vil si at pasienten ikke skal ha spist, drukket eller røyket de siste 12 timene. Eksempler på analyser som krever faste er triglyserider, glukose, glukosebelastning, laktosebelastning, C-peptid, insulin og gallesyre. Se Analyseregister.
7.1.2 Legemiddelfaste
Prøver til legemiddelanalyser skal tas medikamentfastende, det vil si før pasienten inntar neste dose.
7.1.3 Kroppsstilling ved prøvetaking
Pasientens kroppsstilling under prøvetaking påvirker konsentrasjonen av høymolekylære stoffer, blodceller og proteinbundne komponenter. Konsentrasjonen er høyere i stående enn i liggende stilling. Pasienten skal sitte eller ligge i ro i minst 15 minutter før blodprøvetaking.
7.1.4 Fysisk aktivitet
Fysisk aktivitet kan påvirke blodprøveresultater. Pasienten skal unngå harde fysiske påkjenninger i dagene før prøvetaking.
7.1.5 Stress
Stress og uro i forbindelse med blodprøvetaking kan påvirke konsentrasjonen av ACTH, kortisol, prolaktin og katekolaminer, samt øke nivået av leukocytter og glukose. Prøvetaking skal derfor gjennomføres med minst mulig stress for pasienten.
7.2.6 Tidspunkt for prøvetaking
Noen analyser har betydelig døgnvariasjon, for eksempel jern og kortisol. Ved gjentatte prøver på samme pasient skal prøvetakingstidspunktet standardiseres. Blodprøver bør generelt ikke tas rett etter at pasienten har inntatt et fettrikt måltid.
8. Generelle retningslinjer for venepunksjon
Venepunksjon skal utføres hygienisk, raskt og så smertefritt som mulig. Venene i albueregionen er best egnet til blodprøvetaking. Områder med hematom, infeksjoner eller arr etter brannskade eller kirurgi skal unngås.
8.1 Arteriovenøs fistel
Blodprøve skal ikke tas fra arm med arteriovenøs fistel.
8.2 Cancer mammae
Nyere forskning viser at blodprøver kan tas i armen på operert side ved brystkreft, da det er nytt og rent utstyr som brukes og prosedyren ikke utgjør noen helserisiko for pasienten.
8.3 Intravenøs væske
Blodprøve skal ikke tas fra en arm med pågående intravenøs væsketilførsel. Dersom prøven likevel må tas, skal infusjonen være stengt i minst 10 minutter før prøvetaking.
8.4 TPN
Ved pågående infusjon med TPN skal infusjonen stenges i minst 15 minutter før blodprøve tas. Det skal ikke tas blodprøver fra annen kroppsdel i denne perioden.
For prøver til triglyserider skal infusjonen være stengt i minst 4 timer før prøvetaking.
Lipid gir interferens på hematologiske og biokjemiske analyser, og skal dermed alltid dokumenteres dersom blodprøven tas samtidig som pasienten får TPN.
8.5 Blodtransfusjon
Ved prøvetaking under pågående blodtransfusjon, gjelder Prøvetaking: Blodprøver til immunologi og transfusjonsmedisin (Ikke tilgjengelig).
9. Forhold på sengeposten
Prøvetakingslister, etiketter og sendeskjemaer inneholder sensitiv pasientinformasjon. Lister og etiketter skal snus eller dekkes til med verneark merket «Til vern om taushetsplikt», som skal ligge på alle traller.
I noen tilfeller blir sengehest, nattbord, stoler og ringesnor flyttet på for at prøvetaker skal kunne ta blodprøver. Da er det viktig at alt blir satt tilbake, og innenfor pasientens rekkevidde og synsfelt før en forlater rommet.
Hvis pasienten ikke er til stede på rommet, skal personalet kontaktes for assistanse, og det skal eventuelt avtales at prøvene tas ved neste planlagte prøvetakingsrunde.
Ved flytting av pasienten til annen sengepost, skal rekvisisjonen slettes med begrunnelse for annullering. Sengeposten har ansvar for å rekvirere nye prøver til faste runder eller kontakte AMB ved behov for øyeblikkelig hjelp.
Unntatt ved psykiatrisk avdeling:
Rekvisisjoner skal ikke slettes, selv om prøven ikke blir tatt. I stedet skal det dokumenteres tydelig hvorfor prøven ikke ble tatt i Unilab eller i Debra.
-
Rekvisisjonen skal først aktiveres
-
Årsaken til at prøven ikke er tatt skal dokumenteres under «intern lab-kommentar» eller «kommentar til rekvisisjon»
-
Rekvisisjonen skal deretter inaktiveres
10. Sendeprøver til andre laboratorier og sykehus
Blodprøver rekvirert til andre sykehus eller de andre laboratoriene skal bestilles i DIPS Arena. Ved elektroniske bestillinger er papirrekvisisjon ikke nødvendig, så fremt analysen finnes i DIPS Arena.
Bestillinger som krever medfølgende skriftlige kliniske opplysninger (for eksempel prøver til metabolsk screening og medisinsk genetikk) skal alltid ha korrekt utfylt sendeskjema. Skjemaet skal inneholde pasientopplysninger, rekvirentopplysninger og faktisk prøvetakingstidspunkt.
Sendeprøver som ikke tas, kan ikke slettes av AMB. Dette skal dokumenteres i Unilab ved å legge inn «Intern lab-kommentar» med passende forklaring, for eksempel: «Prøve ikke tatt etter avtale med rekvirent».
11. Korrekt ID
11.1 Identifisering av pasienten
-
Prøvetaker skal presentere seg for pasienten og informere om blodprøvetakingen.
-
Prøvetaker har ansvar for å kontrollere at etikettene inneholder: rekvirent, pasientens navn og fødselsnummer, hvilke analyser som er rekvirert, dato og klokkeslett for prøvetaking.
-
Pasienten skal oppgi fullt navn og fødselsnummer. Identifikasjonen skal stemme med opplysningene på prøvetakingsetikettene.
-
Dersom pasienten ikke kan oppgi fullt navn eller fødselsnummer, skal identifikasjon verifiseres via ID-armbånd eller legitimasjon.
-
Hvis pasienten identifiseres av personale på sengepost, skal navnet til den ansatte noteres på prøvetakingslisten, Unilab eller i Debra: «Pasienten er identifisert av _____».
-
Prøvetaker skal registrere seg i Unilab ved å føre inn brukernavn (4–6 tegnskode) under «Prøvetaker».
-
For prøvetaking til pretransfusjonsundersøkelse, følg prosedyre Blodprøver til pretransfusjonsundersøkelse.
11.2 Merking av prøvetakingsrør
Etikett
Etter prøvetaking skal alle rør merkes med prøvetakingsetikett med barkode ved pasientens seng eller stol, før rommet forlates. Etiketten skal snus slik at barkoden står rett under korken. Barkoden må ikke plasseres for langt nede på røret, da dette kan gi avlesningsproblemer på instrumentene.
Pretransfusjonsundersøkelse/blodtyping
For merking av prøver til pretransfusjonsundersøkelse, se Prøvetaking: Blodprøver til pretransfusjonsundersøkelser.
Rémerking av prøver
Ved rémerking skal all informasjon på ny etikett (pasientens navn, fødselsnummer og eventuelt rekvisisjonsnummer) samsvare med eksisterende etikett på prøverøret. Den nye etiketten skal signeres av prøvetaker for å sikre sporbarhet.
Klokkslett
Prøver til APTT, Anti-Xa, ammoniakk, kapillære gelrør, sendeprøver og andre tidssensitive analyser skal merkes med prøvetakingstidspunkt på etiketten.
Dersom oppgitt prøvetakingstid og faktisk prøvetakingstid avviker med mer enn ±45 minutter, skal det oppgitte klokkeslettet strykes, og det faktiske prøvetakingstidspunktet skal skrives manuelt på etiketten.
Unntak gjelder ved bruk av Debra-appen. Når appen benyttes, registreres tidspunktet for innsending av fullført prøvetaking automatisk som nøyaktig prøvetakingstidspunkt. Det er da ikke nødvendig å korrigere klokkeslettet på etiketten manuelt.
12. Prøvetaking
12.1 Utførelse av venepunksjon
- Sjekk bestillingen og finn frem riktige prøverør
- Undersøk om noen analyser krever spesielle forberedelser (se laboratoriehåndboken)
- Utfør håndhygiene
- Identifiser pasienten
- Kontroller at pasienten har god sitte- eller liggestilling, og at armen ligger stødig
- Sett på stasebåndet ca. 10 cm over stikkstedet
- Finn et egnet stikksted
- Vask stikkstedet ved behov (se punkt 6.1: Pasientens sikkerhet)
- Utfør venepunksjonen
- Løsne stasebåndet så snart blodet renner. Staseslangen skal brukes i så kort tid som mulig, og skal ikke være på i mer enn 1 minutt
- Fyll rørene i riktig rekkefølge. Bland hvert rør umiddelbart 3 ganger etter prøvetaking, og deretter 7 ganger etter endt prøvetaking – totalt 10 ganger
- Sikre kanylen umiddelbart med etthåndsgrep
- Sett på tupfer og plaster på innstikksstedet, og trykk uten å bøye armen
- Merk rørene ved pasienten. Prøvetaker har ansvar for at prøven tas fra riktig pasient og at prøvene merkes korrekt. Umerkede prøverør vil bli avvist og kassert
- Kast brukt kanyle i korrekt avfallsbeholder, uten å demontere nål og holder; kastes samlet
- Utfør håndhygiene etter prosedyren
- Gjenværende prøvetakingsetiketter med pasientinformasjon skal makuleres.
Rørrekkefølgen skal følges nøye for å unngå overføring av tilsetningsstoffer (citrat, heparin, EDTA osv.) mellom rørene.
Plakaten viser anbefalt rørrekkefølge ved venøs prøvetaking. Samme rekkefølge gjelder også ved prøvetaking fra kran eller kateter.
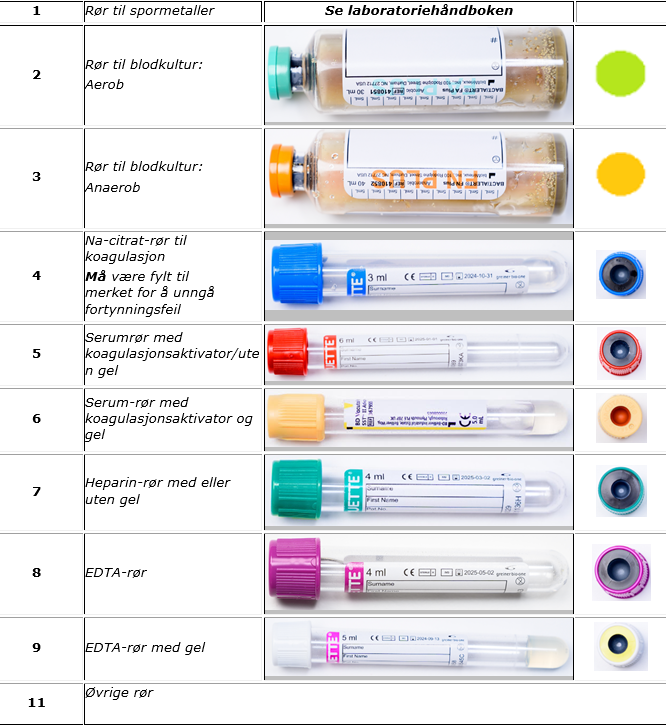
Se også Blodprøvetaking generell veiledning - rekkefølge rør. Plakaten er relatert til dette dokumentet.
12.2 Når skal kasterør brukes
Ved bruk av butterfly
- Dersom første rør er et citratrør, rør til analyser som ionisert kalsium (SICA) eller venøs blodgass.
- Årsaken til at kasterør brukes, er at lufttilførsel i det første røret kan påvirke prøveresultatet. Kasterør er også nødvendig for å sikre korrekt forhold mellom blodmengde og tilsetningsstoff i prøverøret.
Blodprøvetaking fra CVK
- Kasterør brukes også ved prøvetaking fra kateter, som for eksempel CVK.
- Kasterør brukes for å hindre kontaminering av blodprøvene (fortynning eller påvirkning fra infusjonsvæsker/heparin).
Blodprøvetaking fra arteriekran
Ved blodprøvetaking fra arteriekran aspireres blodet først i et lukket system. Sykepleier tar deretter de rekvirerte blodprøvene, og det aspirerte blodet skylles tilbake i systemet etter prøvetaking. Det er derfor ikke behov for kasterør i disse tilfellene.
Valg av kasterør
-
Kasterør bør være av samme type som det første røret som skal tas.
-
Dette sikrer korrekt rørrekkefølge og reduserer risiko for kontaminering av påfølgende prøver.
12.3 Prøvetaking på barn
Venøs prøvetaking på barn utføres som hos voksne. Smertelindring/lokalbedøvelse anbefales.
God kommunikasjon med barnet og barnets foreldre/foresatte er viktig. Fortell barnet om prøvetakingen og tilpass informasjonen til barnets alder. Distraksjoner kan redusere stress i prøvetakingssituasjonen.
Nyfødte og spedbarn har små blodvolum, begrens prøvetakingen i samråd med lege. Se også prosedyre for prøvetaking av nyfødt generell, punkt 5.2.
12.4 Forsendelse av prøver til AMB
-
Bruk rørpost og send prøvene til AMB kontinuerlig, Medisinsk biokjemi: Mottak og forsendelse av rørpost (Ikke tilgjengelig). Dette sikrer raskere blodprøvesvar.
-
Kun prøver til AMB skal sendes til stasjon 104, 090, 102 og 138.
Merking av prøver
-
Skriv klokkeslett på etiketten til sendeprøver for raskere prøvebehandling etter mottak.
-
Dersom sengepostens etiketter benyttes, må dato, klokkeslett og avdeling føres på etiketten.
-
Analyser må være bestilt i DIPS.
Prøver til analyse av immunsuppressiver
Prøver til analyse av immunsuppressiver som sirolimus (Siro), everolimus (Evero), takrolimus (Tacro) og ciklosporin A (Cya) – må ankomme laboratoriet senest kl. 09.00 på hverdager for å få svar samme dag.
13. Preanalytiske feilkilder
13.1 Langvarig stase
Stasen skal være stram nok til å stanse den venøse blodstrømmen, men ikke så stram at den hindrer den arterielle tilførselen.
Stasen bør ikke sitte på i mer enn 1 minutt. Forlenget stase fører til at plasma siver ut fra blodbanen og over i vevet, noe som kan påvirke analyseresultatene.
Stase medfører også lokal oksygenmangel. Økt melkesyremetabolisme kan da føre til acidose og forhøyet kalium (hyperkalemi). Acidosen forsterkes dersom pasienten pumper eller knytter hånden under prøvetaking, og dette kan særlig gi økt kaliumkonsentrasjon.
For å gjenopprette normale forhold etter forlenget stase, må man vente minimum 2 minutter før ny stase settes på.
13.2 Koagulering
Dårlig venepunksjon som gjør at blodet renner sent, kan føre til hemolyse og uønsket koagulering.
Dersom blodet ikke blandes (3+7) tilstrekkelig med tilsetningsstoffene i prøverøret, kan det koagulere. Ved analysering av fullblod, som koagulasjons- og hematologiske undersøkelser, vil prøven da ikke kunne analyseres.
13.3 Hemolyse
Hemolyse innebærer at erytrocyttene sprekker, slik at hemoglobin og andre intracellulære komponenter frigjøres til plasma eller serum. Dette kan føre til falskt forhøyede analyseresultater, særlig for stoffer som normalt finnes i høy konsentrasjon inne i cellene.
-
Kalium
-
LD (laktatdehydrogenase)
-
ASAT
-
ALAT (i mindre grad enn ASAT)
-
CK
-
Fosfat
-
Magnesium
-
Jern
I tillegg kan hemolyse interferere analytisk (optisk interferens) og påvirke flere andre analyseresultater.
De vanligste årsakene til hemolyse ved blodprøvetaking er:
-
For langvarig eller for stram stase
-
Pasienten pumper eller knytter hånden under prøvetaking
-
"Roting"/vanskelig venepunksjon
- Høyt vakuum i prøverør kombinert med tynn kanyle
-
Risting av prøverøret (røret skal vendes forsiktig, ikke ristes)
-
Forsinket sentrifugering eller feil oppbevaring/transport
13.4 Sentrifugering
Prøverør som brukes til fremstilling av serum, må separeres fra blodcellene innen 2 timer etter prøvetaking. Det er derfor viktig at korrekt prøvetakingstidspunkt alltid fremgår på etiketten. Bruk Debra eller skriv på etiketten manuelt dersom prøvetakingstidspunktet avviker med +/- 45 minutter.
Dersom prøven blir stående for lenge før sentrifugering, vil stoffutveksling mellom blodceller og serum kunne endre konsentrasjonen av flere analytter. Resultatene vil da ikke lenger være representative for pasientens reelle verdier.
13.5 Blanding
Prøverørene må blandes forsiktig for å sikre korrekt prøvekvalitet:
-
Bland røret 3 ganger straks det tas ut av holderen.
-
Bland deretter alle rør ytterligere 7 ganger etter at prøvetakingen er fullført, totalt 10 ganger.
Ved fullblodsanalyser er det spesielt viktig at hele innsiden av røret dekkes med blod, slik at tilsetningsstoffene løses opp umiddelbart og blodet ikke koagulerer.
Ikke tilstrekkelig blanding kan føre til:
-
Koagel i prøven - blodet har koagulert, ofte på grunn av manglende eller utilstrekkelig blanding med antikoagulant.
-
Dårlig homogenitet - prøven er ikke godt blandet, noe som kan gi uriktige analyseresultater.
-
Sedimentering av røde blodcellene - cellene har sunket til bunnen, noe som kan påvirke konsentrasjonen av analyttene i plasma/serum.
13.6 Vanlige preanalytiske feil
-
Ufullstendig eller manglende pasientidentifikasjon
-
Mangel på samsvar mellom rekvisisjon og prøve
-
Feil prøvemateriale eller prøvetakingsrør
-
Manglende eller feil dato og tidspunkt for prøvetaking
-
For gammelt prøvemateriale
-
Feil prøvevolum (f.eks. for lite blod i citratrør)
-
Koagulert prøve (gjelder f.eks. hematologi- og koagulasjonsanalyser)
-
Feil oppbevaring av prøverør (lys og temperatur)
-
Prøverør utgått på dato
-
Hemolyse i prøven (avhengig av analyse og grad av hemolyse)
-
Lipemi i prøven
-
Prøve tatt på feil tidspunkt (gjelder legemiddel- og hormonanalyser)
Dette er de vanligste årsakene til at prøver ikke kan analyseres eller gir feil resultater.
14. Prøvetaking uten bestilling
14.1 På sengepost
Dersom man mottar en muntlig forespørsel om blodprøver, skal prøvetaker alltid be sykepleier eller lege om å rekvirere analysene umiddelbart i DIPS.
Prøvetaker kan først ta blodprøven når skriftlig bestilling foreligger, enten i form av prøvetakingsetiketter eller prøvetakingsliste.
14.2 Akutt mottak
Akutte prøvetakingssituasjoner
Ved akutte situasjoner – som traume, kritisk syk voksen/barn eller trombolyse – tas blodprøver ofte før sykepleier rekker å rekvirere i DIPS.
-
Kommuniser alltid med teamleder/sykepleier om hvilke prøver som skal tas.
-
Alle prøver må merkes med korrekt pasient-ID, bruk navneetiketter.
-
Påfør prøvetakingsdato, klokkeslett og signatur på prøver til blodbanken.
-
Husk ferdig utfylt B-bank-skjema til Avdeling for immunologi og transfusjonsmedisin.
Blodprøverør ved akutte situasjoner
Traume: citratrør, serumrør med gel, EDTA-rør, rør til B-bank 1 - spør teamleder om B-bank 2 skal tas
Kritisk syk voksen/barn: citratrør, serumrør med gel, EDTA-rør, rør til B-bank 1 og i noen tilfeller er det nødvendig med blodkultur - spør teamleder om B-bank 2 skal tas
Trombolyse: citratrør, serumrør med gel, EDTA-rør, rør til B-bank 1- spør teamleder om B-bank 2 skal tas
15. Avfallshåndtering
-
Alle kanyler skal sikres forsvarlig før de kastes i gule avfallsbokser for stikkende og skjærende avfall.
-
Bytt avfallsboksen når den er ¾ full. Press ned luken på lokket til det høres tre klikk.
-
Sett på etikett merket "Smittefarlig avfall til forbrenning" og kryss av for "Stikkende/skjærende avfall".
-
Merk etiketten med avdeling, dato og signatur.
-
Brukte eller åpne glass med blod skal kastes i beholder for biologisk avfall.
16. Annet
Blodprøvetaking fra arteriekran, hickman, VAP, CVK eller PVK
-
Hvis kommentarfeltet angir at prøven kan tas fra arteriekran, Hickman, VAP, CVK eller PVK, skal rørene merkes med etiketter og legges i et pussbekken sammen med adapter og eventuelt kasteglass. (Merk: arteriekran bruker ikke kasteglass.
-
Pussbekkenet med utstyr leveres til sykepleier eller settes på avtalt plass.
-
OBS! Citratrør med delvolum (2 ml) kan ikke brukes til tapping fra arteriekran, da arterietrykket overfyller glasset.
-
Dokumenter i Unilab eller Debra at prøven er tatt fra arteriekran/Hickman/VAP/CVK/PVK.
Ved vanskeligheter
-
Hvis prøvetakingen ikke lykkes etter 2–3 forsøk, eller man ikke får tilstrekkelig antall prøverør, skal en anne prøvetaker hentes for å forsøke.
-
Dersom pasienten motsetter seg prøvetaking, skal avdelingens personale kontaktes. Det er personalet som avgjør om prøvene skal tas eller ikke.
17. Avvik
Avvik skal rapporteres i Synergi.
18. Kilder/referanser
- Blodprøvetaking - venøs
- EFLM Recommendation for venous blood sampling
- Helsebiblioteket.no
- Husøy, AM (red.) Blodprøvetaking i praksis 3. utgave, Oslo: Cappelen Damm Akademiske, 2018
- Spesialisthelsetjenesteloven (1999). Kapittel 6. Taushetsplikt, opplysningsplikt og veiledningsplikt. Tilgjengelig fra https://lovdata.no/lov/1999-07-02-61. (Lastet ned 16.06.20)
- Hematologi: Fyllingsgrad i EDTA-glass og varsling av prøver med koagel.